CRISPR-Cas12f1: Mini nástroj pro úpravu genomu
Informace organizace BIOTRIN

Výzkumníci a partneři ShanghaiTech University oznámili nový nástroj pro úpravu genomu s názvem Cas12f1. Výsledky své práce publikovali v časopise Nature Chemical Biology.
Nukleázy spojené s CRISPR (Cas) řízené RNA jsou velmi užitečné nástroje pro úpravu genomu u různých druhů. Velká velikost běžně používaných nukleáz Cas9 a Cas12 však omezuje jejich použití, zejména pro terapeutické účely. Efektory Cas9 a Cas12a řízené RNA mají totiž většinou více než 1 000 aminokyselin a tato velikost přináší obtíže pro jejich účinné sbalení do vektorů, které fungují s omezenou velikostí inzertu, jako jsou třeba adenoviry (AAV), jedny z nejpoužívanějších virů pro přenos genů. Kompaktnější systémy by mohly nabídnout širší terapeutické využití a více možností v této oblasti.
Ze známých systémů Cas12f vědci v uvedené práci vybrali pro komplexní analýzu miniaturní systém pro úpravu genomu CRISPR-Cas třídy 2 typu V-F z Acidibacillus sulfuroxidans (AsCas12f1). AsCas12f1 je endonukleáza řízená RNA, která generuje v cílové DNA dvouvláknové zlomy. Je tvořena 422 aminokyselinami, což je méně než polovina velikosti většiny efektorů Cas9 a Cas12. V článku jsou shrnuty výsledky systematické charakterizace biochemických vlastností tohoto miniaturního efektorového proteinu.
Vědci prokázali, že komplex AsCas12f1-crRNA-tracrRNA účinně štěpí dsDNA cíle, pokud je rozpoznán PAM (motiv sousedící s cílovou sekvencí neboli protospacerem, angl. protospacer adjacent motif) bohatý na 5′ T a jeho navazující okolí se shoduje s vodicí sekvencí v CRISPR RNA (crRNA). Jeho působením vznikají asymetrické stupňovité dvouřetězcové zlomy DNA (DSB). Ukázali, že AsCas12f1 může být účinný nástroj pro úpravu genomu v bakteriích (Escherichia coli a Klebsiella pneumoniae), jakož i v různých lidských buňkách prostřednictvím různých metod přenosu, včetně plazmidu, ribonukleoproteinu (RNP) a AAV.
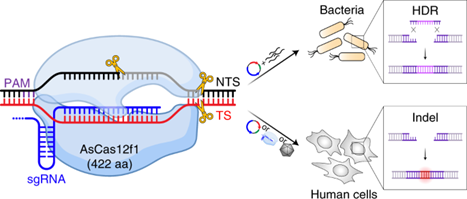
Obr.1: Schéma štěpení dsDNA zprostředkované AsCas12f1
Hodnotili také přesnost editace AsCas12f1 pomocí neshodných naváděcích sekvencí – jedno nebo dvou-nukleotidové neshody podstatně snížily indelovou aktivitu AsCas12f1 na endogenním lokusu, což naznačuje, že AsCas12f1 vykazuje dostatečnou editační přesnost (pozn.: indel mutace spočívají v inzerci nebo deleci několika párů bází do/ze sekvence). Pomocí sekvenace byl odhalen další rys – indely vyvolané AsCas12f1 se vyskytovaly hlavně na distálním konci protospaceru a významná část indelů zachovala cílové místo neporušené, změnila se pouze sekvence za ním. Na rozdíl od procesu editace genů zprostředkovaného Cas9, při němž většina indelů generovaných nehomologním spojováním konců (angl. Non-homologous end joining, NHEJ) narušuje cílové místo, mohou být editace vyvolané AsCas12f1 iterativně zaměřeny stejnou vodicí RNA, dokud není cílové místo odstraněno homologicky řízenou opravou (angl. homology directed repair, HDR) nebo delecí dlouhé sekvence.
Souhrnně tato data vytvořila základ pro pochopení mechanismu štěpení dsDNA miniaturními nukleázami Cas12f a stanovila aplikační potenciál AsCas12f1 jako nástroje pro editaci genomu.
Tato práce by tedy mohla pomoci dalším výzkumníkům vytvořit kompaktnější nástroje pro úpravu genomu. Už jsou o to první snahy – v jiném článku výzkumníci z pákistánského Národního institutu pro biotechnologii a genetické inženýrství zkoušeli systém CRISPR-Cas12f1 při vývoji upravených rostlin bez transgenů s použitím nanočástic a virů jako vektorů.
Zdroje:
- https://www.isaaa.org/kc/cropbiotechupdate/article/default.asp?ID=19119
- https://www.nature.com/articles/s41589-021-00868-6
- https://www.sciencedirect.com/science/article/pii/S1360138521003083#
Zdroj: BIOTRIN










